gamma gaz monoatomique – gaz monoatomique et diatomique
Théorie cinétique des gaz
TD corrigés de thermodynamique
· Fichier PDF
Définition: Fonction de partition du gaz parfait monoatomique Puisque V N r N = 0 et nous pouvons calculer indépendamment les intégrales concernant les coordonnées spatiales r i : Puisqu’il y a N particules i de coordonnées r i , nous aurons V N et nous obtenons :
loi de Laplace thermodynamique
vitesse du son pour un gaz monoatomique
le cas monoatomique où la forme de Cv et de Cp est une constante Cv=3/2R et Cp=5/2R dans les autres cas gamma n’est pas simple et dépend de T , l’équation d’état du gaz parfait étant PV=nRT => T=PV/nR gamma dépend de PV , ainsi je n’arrive pas à comprendre comment l’intégration
Un gaz monoatomique est un gaz dont les constituants sont des atomes isolés Dans un sens plus restreint l’expression gaz monoatomique désigne un corps simple élémentaire à l’état gazeux monoatomique c’est-à-dire un gaz dont les atomes isolés sont tous du même élément chimique Ils se répartissent en trois types: les gaz nobles: He, Ne, Ar, etc, Ces éléments sont gazeux et …
Temps de Lecture Estimé: 2 mins
Indice adiabatique — Wikipédia
Vue d’ensemble
Du gaz parfait monoatomique aux phases condens´ees
· Fichier PDF
L’hypothèse des gaz parfaits cp et cv constants n’est en toute rigueur vérifiée que pour les gaz monoatomiques qui ne comportent aucun mode de rotation ni de vibration moléculaire, Elle est d’autant moins satisfaisante que la molécule de gaz comporte davantage d’atomes et donc de modes vibratoires possibles, La thermodynamique statistique permet de déterminer les valeurs des
Initiation à la thermodynamique moléculaire pour le génie
Gaz parfaits et idéaux
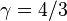
Gaz monoatomique — Wikipédia
gamma gaz monoatomique
pour un gaz diatomique E = 5 2, n, mol, RT donc C, V = 5 2, n, mol, R, Pour le gaz monoatomique, comme l’enthaphie totale est E +PV = 3 2, n, mol, RT +n, mol, RT soit donc pour la capacit´e calorifique : C, P = 5 2 n, mol, R, Pour un gaz diatomique C, P = 7 2, n, mol, R, On note γ = C, p /C, v, il passe de pour l’air γ = 1,4, Pour un gaz parfait on voit que l’on a a C, p, −C, V = n, mol, R, et C, V = n, mol, R …
Premier et Second Principes
· Fichier PDF
Gaz monoatomique
Gaz parfait monoatomique Dans le cas d’un gaz parfait monoatomique, on suppose que la totalité de l’énergie est sous forme d’énergie cinétique des molécules énergie thermique, donc l’ énergie interne U du système vaut :
Initialement connus en tant que “gaz inertes” puis “gaz rares” ce qui n’est pas tout à fait exact pour plusieurs d’entre eux ils furent ensuite appelés “gaz nobles” L’appellation ” gaz monoatomiques ” est une autre appellation possible pour cette famille d’éléments qui sont tous gazeux et monoatomiques dans les conditions standard de température et de pression
· La vitesse du son dans un gaz est: où P est la pression, rhô la densité et gamma le coefficient adiabatique du gaz, Pour un gaz monoatomique gamma vaut …
La gammapathie monoclonale GM est définie par la présence dans le sérum et/ou les urines d’une immunoglobuline monoclonale Elle peut être associée à une hémopathie maligne dans le cas …
Un gaz monoatomique est un gaz dont les constituants sont des atomes isolés [a], Dans un sens plus restreint, l’expression gaz monoatomique désigne un corps simple élémentaire à l’ état gazeux monoatomique, c’est-à-dire un gaz dont les atomes, isolés, sont tous du même élément chimique [ b ] ,
2 Th´eorie cin´etique du gaz parfait monoatomique GPM 21 Le mod`ele du GPM Un gaz est monoatomique s’il est constitu´e d’atomes ex : gaz rares La plupart des gaz sont polyatomiques c’est-`a-dire qu’ils sont constitu´es de mol´ecules Le mod`ele du GPM : i le GPM est constitu´e d’atomes identiques, ponctuels et sans interaction
Gaz monoatomiques : présentation
1 Théorie cinétique du gaz parfait monoatomique : a Effusion calcul approché : un récipient de volume V 0 = 1 L, maintenu à température constante égale à 0°C, contient de l’hélium sous la pression P 0 = 1 mm Hg, A l’extérieur du récipient règne le vide, On note n = N / …